Das Bikarbonat-Mangel-Syndrom (BDS)
Tägliche Bikarbonat-Substitution, Wirkung und Nutzen für Wohlbefinden und Gesundheit im Allgemeinen und in der Medizin.
Emer. Prof. Dr. med. K.F. KOPP II. Med. Klinik r. d. Isar, Technische Universität München
Stand: 21.02.2014
Zusammenfassung
Verschiedentlich wird zur "Verbesserung" des Säure-Basen-Haushalts die Zufuhr von Natriumbikarbonat, Synonym Natriumhydrogenkarbonat, Natron, Baking-Soda (chemische Formel NaHCO3) oder anderer alkalisierender Substanzen empfohlen. Dosierungsanleitungen sind dabei äußerst vage. Ein unterschiedlicher Bedarf von Personen mit unterschiedlichem Stoffwechsel und unterschiedlicher Nierenfunktion, Gewicht oder Alter konnte bislang auch nicht quantitativ definiert werden.
In der Medizin gibt es für die Behandlung besonders von Nierenkranken besondere Indikationen für Natriumbikarbonat, sei es durch intravenöse Infusion oder auch in Form besonderer Tabletten oder Kapseln.
Wegen der Bedenken gegenüber der damit verbundenen Natrium-Zufuhr wird die Gabe von Natriumbikarbonat gelegentlich noch kontrovers oder vorsichtig, wenn nicht negativ beurteilt. Leider unterliegt diese Anschauung bzw. die Negativ-Beurteilung weltweit einem bedauerlichen, "wissenschaftlichen" Irrtum. (Siehe Anhang)
Aufgrund wissenschaftlich gesicherter physiologischer und biochemischer Erkenntnisse und persönlicher, klinisch-wissenschaftlicher Erfahrungen des Autors ist der Nutzen einer Substitution von Natriumbikarbonat sowohl für die allgemeine Gesundheit als auch zur Prophylaxe und Therapie der verschiedensten Krankheitsbilder in der Medizin außerordentlich hoch. Häufig liegt beim älteren Gesunden aus nierenphysiologischen Gründen, immer aber im Krankheitsfall auch ein pathologisch niedriger Bikarbonat-Blutspiegel vor.
Basierend auf der zentralen Rolle des Säure-Basen-Haushaltes im Stoffwechsel des Organismus und aufgrund noch wenig bekannter Verknüpfungen mit der Durchblutung d.h. mit der Sauerstoffversorgung der Organe, könnte daher in Zukunft nicht nur in der Medizin, sondern aus allgemein gesundheitlichen und damit aus sozio-ökonomischen Gründen ein überraschend steigender Gebrauch von Natriumbikarbonat z.B. in Form von Nahrungs-Ergänzungsmitteln oder Getränken entstehen.
Einleitung: Physiologische Grundlagen
Unsere Körpertemperatur von 37.5° Celsius ist uns als eine normalerweise physiologische, gleichbleibende Konstante vertraut, d.h. wir sind iso-therm. Eine weitere physiologische Konstante des Organismus ist der Parameter für den Säure-Basen-Haushalt der pH-Wert im Blut. Dieser wird in einem außerordentlich engen Bereich zwischen pH 7.35 und 7.45 durch Puffer-Systeme exakt konstant gehalten. Der Mensch ist daher wie alle (Land)-Säugetiere auch ein Iso-pH-Lebewesen oder ein pH-Homöostase-Lebewesen. Ohne die Konstanz des pH - bzw. des Säure-Basen-Gleichgewichts ist der richtige Ablauf der biologischen und biochemischen Prozesse im Inneren des Organismus nicht gewährleistet.
Darauf hat bereits im Jahr 1860 der "Ur-Vater" und Begründer der experimentellen Physiologie, der große französische Wissenschaftler und Forscher Claude Bernard (1813 – 1878) hingewiesen (Abb. 1).
Zitat: "Die Konstanz des - Milieu interieur - (= Homöostase) ist die Voraussetzung für ein von der Umwelt unabhängiges und freies Leben".
Insgesamt gewährleisten vier Puffersysteme des Blutes die Konstanz des Blut-pH-Wertes. Mit knapp 75 % der gesamten Pufferkapazität steht dabei das Kohlensäure-Bikarbonat-System an erster Stelle. Die wichtigste natürliche Puffersubstanz des Blutes ist daher das Natrium-Bikarbonat (Na+HCO3-). Hämoglobin- (mit circa 25 %), Proteinat- (mit circa 1 %) und Phosphat-Puffer (mit < 1%) vervollständigen die Gesamt-Pufferkapazität des Blutes.
Beim jungen, gesunden Menschen wird das Säurebasen-Gleichgewicht im Organismus vor allem dadurch konstant erhalten, dass die Nieren (assistiert von den Lungen durch Abatmung von CO2), die täglich im Stoffwechsel entstehenden Säuren (bei einem Körpergewicht von ca. 70 kg sind es ca. 50 – 80 mMol/Tag) vermittels des sauren Urins ausscheiden. Gleichzeitig wird die Blut-Bikarbonat-Konzentration durch die Nieren-Tubulus-Zellen vermittels Rückresorption von Bikarbonat aus dem Primärharn und durch Neusynthese aus CO2 und H2O auf dem physiologischen Niveau von 25 mMol/L konstant gehalten.
Es ist daher leicht zu verstehen, dass bei Patienten mit Nierenerkrankungen und verminderter Nierenleistung auch Probleme mit dem Säure-Basen-Haushalt auftreten, d.h. es kommt zu einem Bikarbonat-Mangel und damit zur Übersäuerung (= Azidose) des Organismus. Die erkrankte Niere kann weder die anfallenden Stoffwechselsäuren im notwendigen Maße ausscheiden, noch kann sie dem Organismus ausreichend Bikarbonat zurückgewinnen, um die neutrale pH-Konstanz zu erhalten. Das Wie und Wieso gehört in das spezielle Gebiet der Patho-Physiologie der Nieren-Erkrankungen.
Beim Gesunden verursacht schon der natürliche, physiologische Alterungsprozess eine Verminderung der Nierenleistung. Es entsteht früher oder später eine Azidose. Der altersbedingte Leistungsverlust der Nieren kann mit der sog. Cockcroft-Formel genau berechnet werden. Sehr früh, schon nach dem 25. Lebensjahr nimmt die Leistung der Nieren kontinuierlich ab und beträgt zwischen dem 60. und 70. Lebensjahr nur noch maximal 50 % der jugendlichen Nierenleistung.
Zwar wäre durch eine einseitige vegetarische Ernährung eine Alkalisierung des Organismus u.a. durch Citrate, die zuerst im Körper zu Bikarbonat verstoffwechselt werden, möglich (ca. 60 mMol/Tag), doch drohen, wie bei jeder einseitigen Ernährung, Eiweiß- Vitamin- oder andere Mangelerscheinungen, z.B. Beri-Beri bei Reisbauern in China und Indien.
Zudem braucht der Körper auch bei rein vegetarischer Ernährung dringend Eiweiß = Protein = Aminosäuren (Bedarf, Erwachsene im Durchschnitt 0.59 g/kg KG) bei vegetarischem Eiweiß sogar mehr, um den eigenen Eiweiß-Stoffwechsel ausreichend zu bedienen. Alle Eiweiße enthalten Schwefel, Phosphor, Stickstoff, die als schwefelsaure Metaboliten, als Sulfate, als Phosphate, als Harnstoff und Harnsäure durch die Niere ausgeschieden werden müssen.
Dementsprechend beträgt unser durchschnittlicher täglicher Säureanfall im Körper bei einem 70 kg erwachsenen Menschen ca. 40 bis 80 mMol/Tag, sehr oft auch mehr. Dies ist nach dem 25. Lebensjahr selbst für gealterte, völlig gesunde Nieren zu viel, warum? Der Homo heidelbergensis wurde maximal 25 bis 30 Jahre alt. In dieser kurzen Lebensspanne hatte er 100% Nierenfunktion. Seine zerebrale Weiterentwicklung führte ihn zum heutigen Zivilisationsmenschen. Seine Nieren haben sich in Funktion und Anatomie nicht weiterentwickelt. Vor ca. 500.000 Jahren lebte er als Jäger und Sammler in einer völlig anderen Umwelt. Unsere noch von damals stammenden Steinzeit-Nieren sind in der heutigen Zivilisations-Umwelt völlig überfordert: Durch über-reichliche Ernährung mit Fleisch/Fisch/Milchprodukten, d.h. durch Luxuskonsum von Eiweiß, dazu Genussmittel z.B. Alkohol, durch psychische, gesellschaftliche, berufliche, sportliche oder sonstige Höchstleistungen, siehe unten, durch life-style-Zwänge, Hungerdiäten und Termin-Zeit-Stress, nicht zu vergessen Krankheiten mit Fieber oder Malignomen und deren Therapie mit Zytostatika oder Strahlen, entsteht durch die gesteigerte Stoffwechsel-Aktivität ein noch viel höherer Anfall von sauren Stoffwechsel-Endprodukten wegen eines erhöhten Zerfalls von Eiweißen (Protein-Katabolie). Diese müssen via Niere ausgeschieden werden. Diese hohen Anforderungen für einen ausgeglichenen Säurebasen-Haushalt könnte nur eine völlig gesunde jugendliche Niere erfüllen. Das Bikarbonat-Mangel-Syndrom (BDS) resultiert aus einem Ungleichgewicht aller obengenannten Einflüsse und dem Nierenalter.
Dies ist nichts Neues. Schon in früheren Jahrhunderten wurde dies in den privilegierten Adelsschichten sichtbar, deren typische Erkrankung durch Luxuskonsum von Fleisch die Harnsäure-Gicht, die Podagra war. Die moderne Zivilisations-Gesellschaft leidet nunmehr ebenfalls aufgrund einer zu niedrigen Nierenleistung gegenüber einer permanent meist zu hohen Eiweiß-Zufuhr oder einem gesteigerten Eiweiß-Stoffwechsel (Katabolie durch Sport oder Krankheit) chronisch an einem mehr oder weniger großen Bikarbonat-Defizit und ist chronisch azidotisch. Die Folge: eine Unzahl von Zivilisationskrankheiten.
Die vielen naturheilkundlichen und Apotheken-gängigen Traktate, die sich dem Thema der „Verbesserung“ des Säure-Basen-Haushalts widmen, sind ein Beleg dafür, dass das Problem erahnt wird. Aber leider wird nirgendwo gesagt, welcher pH-Wert im Körper oder in welcher Körperflüssigkeit auch immer, empfehlenswert oder gar auf die Dauer gut sei.
Aufgrund der verschiedenen Möglichkeiten durch Einnahme von Bikarbonat in Pulver- oder Tablettenform evtl. auch mithilfe von besonders Karbonat-haltigen Mineralwässern oder Drinks, den Säure-Basen-Haushalt des Organismus zu verbessern, wird der Autor im Folgenden die auf wissenschaftlichen Ergebnisse und Erfahrungen beruhende einfache Antwort bezüglich des anzustrebenden pH-Optimums geben.
Wissenschaftliche Klassiker
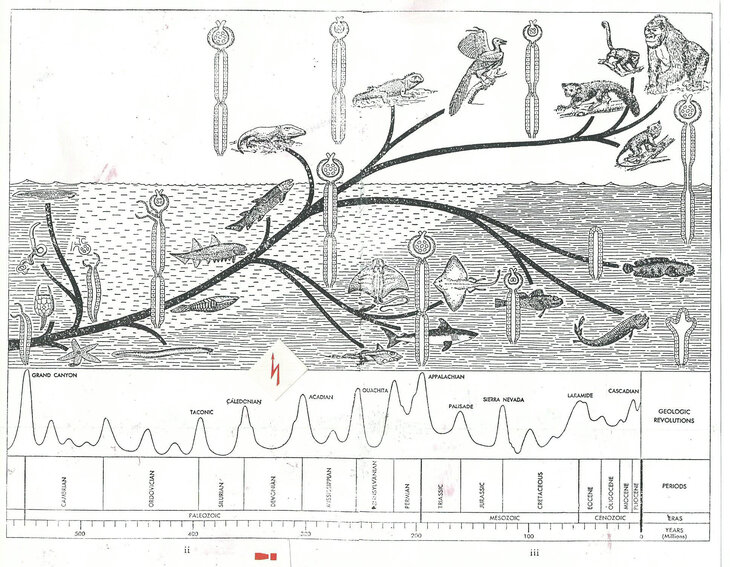
Zum fundierten Verständnis der Rolle von Bikarbonat im Organismus sollen hier noch weitere historische und wissenschaftliche Großtaten erwähnt werden. Der geniale amerikanische Physiologe Homer Smith (1895 – 1962) erforschte in seinem Meeres-Laboratorium auf Long Island (vor New York, USA) durch vergleichende Untersuchungen die Nierenfunktion von niedrigen Organismen über Fische bis zu Säugetieren (Abb. 2).
Er beschrieb die Niere als das Organ, das für die Homöostase (Claude Bernard) aller Organismen, die überhaupt Nieren haben, verantwortlich ist. Nur mithilfe dazu befähigter Nieren konnten Amphibien und frühe Säugetiere in der Devon-Karbonzeit das damals reichlich Bikarbonat-haltige Wasser des Urmeers verlassen, in ihrem Blutkreislauf mitnehmen und so zum Landleben übergehen, so wie es auch für uns Menschen noch immer der Fall ist (Abb. 3).
Durch seinen Selbstversuch, bei dem R.F. Pitts sich und zwei seiner Mitarbeiter (Ayer und Schiess) Bikarbonat intravenös infundierte und die Blutspiegel und die Ausscheidung im Urin gemessen hat, konnte er zeigen, was er schon 1949 im J. clin. Invest. publizierte. Es handelt sich um den in Abb. 6 dargestellten Überlaufmechanismus für Bikarbonat in der Niere (modifiziert und mit ergänzenden Bezeichnungen versehen nach Kopp).
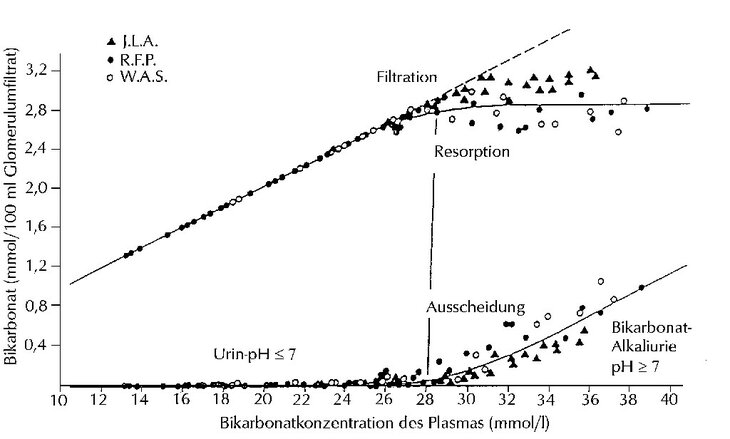
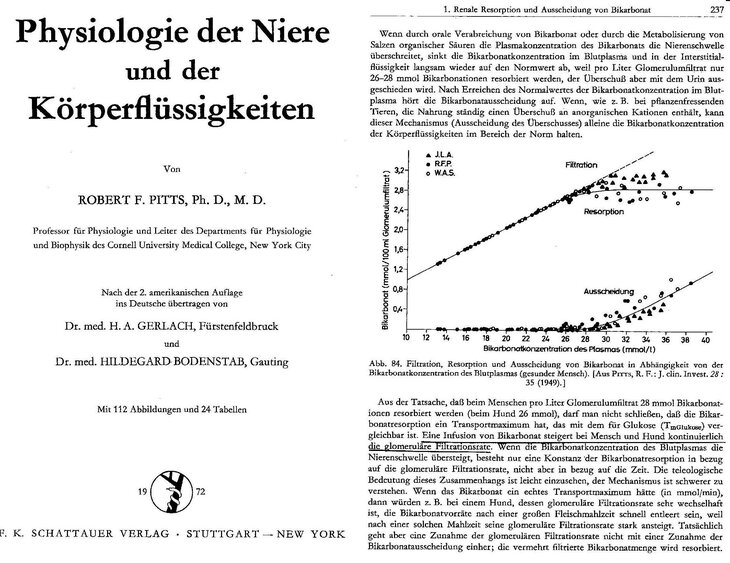
Abbildung 7 zeigt Titelseite und Seite 237 der deutschen Auflage des brillanten Lehrbuchs der Physiologie der Niere und der Körperflüssigkeiten von Robert F. Pitts.
Dieses Lehrbuch hat seit Jahren keine Neuauflage mehr erlebt und ist aus dem Lehrmittelkatalog unserer Universitäten und damit aus dem Wissen und Denken der universitären Nephrologie verschwunden. Statt dessen befassen sich die dort Lehrenden und die dort Lernenden mit der Funktionsweise und der Technologie von Dialyse-Geräten.
Der Körper aller Säuger, so auch der Mensch verfügt also über einen in den Nieren vorhandenen Überlaufmechanismus für Bikarbonat . Wenn die Bikarbonat-Vorräte im Körper voll, bzw. übervoll sind, scheidet die Niere bedingt durch maximale Gefäßerweiterung, die erhöhten Blut-Bikarbonat-Mengen sofort wieder aus und reguliert den Spiegel auf den Normalpegel von ca. 25 mMol/L ein, wodurch dieser konstant gehalten wird ( = pH-Homöostase) wie eingangs beschrieben.
Der praktische Nutzen dieser Entdeckung wird bis heute noch nicht in der Medizin wahrgenommen, geschweige denn therapeutisch angewandt.
Ein weiterer Meilenstein wurde während der 60er Jahre und nachfolgend im Physiologischen Institut der L.M.-Universität München gelegt. Jürgen Schnermann erkannte den in der Niere funktionierenden Rückkopplungs-Mechanismus zwischen Gefäßdurchblutung, Urinmenge und deren Gehalt an NaCl bzw. Natriumbikarbonat. Unter dem Namen des Institutsleiters, Prof. Dr. Klaus Thurau, wurde der sog. Thurau-Mechanismus wissenschaftlich weltweit anerkannt. Damit ist erwiesen, dass zwischen arterieller Gefäßdurchblutung, d.h. der Sauerstoffversorgung des Gewebes und dem Säure-Basen-Haushalt ein Zusammenhang besteht: d.h. je geringer die Azidose, umso besser ist die Gewebe-Durchblutung.
Die tatsächlich im Körper bzw. im Blut vorhandenen Bikarbonat-Reserven sind naturgemäß nicht bekannt, da der Körper nicht wie ein Automobil für Treibstoff oder Öl einen Füllstands-Anzeiger für Bikarbonat hat. Zudem sind die Vorräte von Tag zu Tag verschieden durch die wechselnden Beanspruchungen des Körpers. Wegen der geschilderten, wechselnden Beanspruchung des Körpers wäre dies aber sehr wissenswert - aber wie? Das Problem ist aber relativ einfach dadurch lösbar, indem dem Körper laufend so viel Bikarbonat zugeführt wird, dass immer entsprechend dem Pitts'schen Überlaufmechanismus ein wenig davon im Urin erscheint. Das kann man ganz einfach mittels pH Teststreifen messen.
pH-Messung
Deshalb lautet die KOPP’sche Vorgehensweise und Anweisung: Möglichst bei jedem Wasserlassen, routinemäßig den Urin-pH testen.
Der Urin ist die am besten zugängliche Körperflüssigkeit, welche auch die Verhältnisse im Inneren des Organismus wiederspiegelt. Dies heißt aber keineswegs, dass z.B. der pH im Urin gleich dem pH-Wert des Blutes wäre. Der Urin ist ein hoch konzentriertes Ausscheidungsprodukt mit dem die Nieren "unerwünschte" Stoffwechsel-Endprodukte aus dem Blut bzw. dem Organismus entfernen. Im Fall von Bikarbonat wird ein Überschuss, der oberhalb des physiologischen Normwerts im Blut von 28 mmol/l liegt, sofort mit dem Urin ausgeschieden.
Wenn der Urin sauer ist, heißt dies daher nicht, dass auch das Blut sauer ist. Es heißt nur, im Blut ist nicht ausreichend Bikarbonat vorhanden, dass davon etwas in den Urin gelangen kann. Je größer der Bikarbonat-Mangel im Blut ist, umso saurer ist der Urin. Der niedrigste pH-Wert, d.h. der "sauerst" mögliche Urin beim gesunden Menschen liegt bei einem pH von 4.5. Saurer kann die gesunde menschliche Niere die auszuscheidenden Stoffwechsel-Säuren im Urin nicht konzentrieren.
Bei Nierenerkrankungen mit Minderung der Nierenfunktion ist typischerweise auch die Konzentrationsfähigkeit der Nieren für Säuren stark eingeschränkt. Der Urin-pH liegt dann entsprechend höher im Bereich von pH 6.5. Dies verleitet zu dem Fehlschluss, dass keine schwere Azidose vorliegt, was aber falsch ist. Gerade bei Nierenerkrankungen liegt meistens eine schwere Azidose vor. Direkt kann diese nur durch Messung im Blut festgestellt werden.
Basisch oder alkalisch kann der Urin maximal bis zu einem pH von 8.0 werden, da im Körper keine "Chemikalien" vorkommen, die einen pH von über 8.0 erreichen. Vereinfacht ausgedrückt bedeutet pH die Wasserstoff-Ionen-Konzentration im Kubikzentimeter (= ml) Wasser oder Körperflüssigkeit. Die gesamte pH Skala reicht von 0 = am sauersten, über 7 = neutral, bis zu 14 = maximal alkalisch oder basisch. Zur praktischen Urin-pH Messung sind Test-Streifen geeignet, die den physiologischen Bereich zwischen pH 4 bis pH 8 erfassen und farblich von blass gelb = pH 4 bis tief blau = pH 8 anzeigen. Erhältlich in der Apotheke (Indikatorpapier Uralyt-U Madaus pH 5.6 – 8.0).
Falls kein freies Bikarbonat im Urin festgestellt wird, sollte oral Bikarbonat zugeführt werden.
Obwohl keine allgemeingültige Dosierungsanleitung gegeben werden kann, sind für den Organismus eines nierengesunden 70 kg Menschen je nach Alter mindestens 6 bis 10 Gramm Natriumbikarbonat pro Tag erforderlich um das KOPP’sche Optimum zu erreichen. Menschen mit eingeschränkter oder ohne Nierenfunktion z.B. Dialysepatienten brauchen dagegen mehr, weil die Stoffwechselsäuren nicht ausgeschieden werden.
Erfahrungsgemäß ist also der tägliche Bikarbonat-Bedarf im Einzelfall ohne Messung des Urin-pH überhaupt nicht zu erahnen. Die Messung des Urin-pH kann nur anzeigen, ob und dass der Blut-Bikarbonat-Speicher voll ist oder nicht. Der Urin-pH sagt aber kaum etwas darüber aus wie leer die Speicher sind. Deswegen kommt es nach Einnahme von Bikarbonat immer wieder zu Überraschungen, als würde das zugeführte Bikarbonat spurlos verschwinden. In der Klinik kann dagegen durch genaue Messung des herrschenden Blutspiegels die genaue Menge des fehlenden Bikarbonats festgestellt und durch intravenöse Zufuhr quantitativ genau korrigiert werden.
Der optimale KOPP'sche pH-Bereich im Urin ist pH 7.5 bis 8.0
WARUM?
WEIL: Der enge, normale, physiologische pH-Bereich im Blut liegt zwischen pH 7.35 und 7.45.
Er liegt also nur wenig niedriger als der empfohlene Bereich des Urin-pH von 7.5 bis 8.0 nach Kopp. (Siehe auch Einleitung)
OPTIMAL ist ein Urin pH von 7.5 bis 8.0 deswegen, weil damit noch im Blut vorhandene, überschüssige Bikarbonat-Reserven angezeigt werden, dass davon sogar etwas im Urin erscheint, kenntlich am alkalischen Urin-pH. (Abb. 6)
Dieser Vorrat reicht auch aus, um plötzliche "Sauermacher" z.B. den Milchsäureausstrom aus den Muskeln beim Joggen oder auch drei Whiskeys, kurzfristig zu neutralisieren. Diese Vorräte reichen vielleicht auch noch bis zum nächsten Wasserlassen. Ein Mangel kann dann aber anhand eines Urin-pH < 7.0 sicher festgestellt werden.
Liegt der Urin-pH nach versehentlicher oder absichtlicher Einnahme einer etwas größeren Menge von Natriumbikarbonat auf dem Maximal-Wert von pH 8.0, so ist dies ungefährlich, es zeigt nur an, dass die Nieren überschüssiges Bikarbonat ausscheiden.
Eine Erhöhung des Urin-pH auf pH 8.0 kommt aber auch noch in krankheits-bedingten Fällen z.B. Leberzirrhose oder bei Harnwegs-Infekten mit Harnstoff-spaltenden Bakterien vor. Hierfür sind dann andere basisch wirkende Substanzen z.B. Ammoniak verantwortlich, die den Urin-pH auf 8 erhöhen können. Wenn hierfür also weder die Einnahme von Bikarbonat oder von Calcium- oder Magnesium-Brausetabletten oder eine streng vegetarische Diät verantwortlich gemacht werden kann, ist ärztliche, eventuell klinische Diagnostik zur Aufklärung der Ursache und Therapie erforderlich.
Die berechtigte Frage nach den Gefahren einer Überdosierung von Bikarbonat ist einfach zu beantworten. Bei oraler Aufnahme ebenso wie bei intravenöser Zufuhr von Bikarbonat wird die zu viel ins Blut aufgenommene Menge selbst bei verminderter Nierenleistung sofort wieder mit dem Urin ausgeschieden (Überlaufmechanismus für Bikarbonat in der Niere nach R. Pitts.- siehe Abb. 6).
Nach Einnahme von Bikarbonat als Tabletten oder Pulver kann es im Magen durch die Bildung von Kohlensäure-Gas zu Schaumbildung, Blähungserscheinungen, Aufstoßen sowie Sodbrennen kommen. Bei schwer niereninsuffizienten Patienten ist eine gewisse Vorsicht angebracht. Die Verordnung und Verabreichung von Natriumbikarbonat sollte dann unter ärztlicher Kontrolle erfolgen, wobei der Patient lernen sollte, anhand des Urin-pH die Dosierung selbst zu justieren. Suizidale Überdosierungen erfordern Klinikeinweisung.
Zivilisationskrankheiten bedingt auch durch Bikarbonat-Mangel?
(BDS Bicarbonate-Deficiency-Syndrome, Bikarbonat-Defizit-Syndrom)
Osteoporose, Diabetes, Hypertonie/Bluthochdruck, Nierenschäden bis zur Dialyse.
Schon eingangs wurden die zivilisatorischen Einwirkungen von Umwelt und Ernährung etc. auf den Organismus mit der Folge einer chronischen Azidose, d.h. ein Bikarbonat-Mangel erwähnt. Anders gesagt, die überlebenswichtige Konstanz unseres "Milieu interieur" ist durch eine Mangel-Situation nicht mehr gewährleistet. Die genannten Zivilisationskrankheiten wie z.B. Osteoporose, Diabetes, Hypertonie, Nierenschäden bis hin zur Dialyse und auch Malignome können daher auch als die Folge einer chronischen Azidose gesehen werden.
Osteoporose: Insbesondere die postmenopausale Osteoporose bei Frauen wird durch zusätzliche Hormonmangelzustände verursacht. Diese müssen daher gleichzeitig behandelt werden. Ohne Beseitigung des Bikarbonat- Mangels bleibt die Therapie aber ineffektiv.
Hypertonie/Bluthochdruck.
Wird bei Vorliegen einer Hypertonie auch nach Ausschöpfung sämtlicher diagnostischer Möglichkeiten keine der vielfach möglichen medizinischen Ursache gefunden, spricht man von einer „essentiellen“ Hypertonie. Hierbei bleibt jedoch die bei einer Hypertonie immer vorliegende chronische Azidose, d.h. ein Bikarbonat-Mangel als Ursache außer Betracht und wird als obligates Begleitsymptom betrachtet. Die der Hypertonie zugrunde liegende generalisierte Vasokonstriktion ist jedoch die direkte Folge des NaHCO3-Mangels und wird durch eine Ausschüttung vasokonstriktiver Hormone (Renin-Aldosteron-Angiotension-Kaskade) bewirkt. Therapeutisch werden daher entsprechende „Anti“-Medikamente eingesetzt. Nur der Bikarbonat-Mangel wird nirgendwo beseitigt. Natrium-Bikarbonat wäre dabei die physiologisch am besten wirkende vasodilatatorische Substanz. Tatsächlich gelingt es durch konsequente Bikarbonat-Substitution mit dauerhafter Sättigung der Bikarbonat-Speicher eine Hypertonie wirksam zu therapieren, der Zustand der „alcalotic volume-contractions“ wird hierdurch herbeigeführt.
Malignome und Chemo- oder Strahlen-Therapie. Hierzu existiert eine wissenschaftliche Dissertation
Hirnödem. Posttraumatisch, perioperativ., oder Stoffwechsel-bedingt. (Hangover nach Alkohol-Abusus) Durch Beseitigung einer Bikarbonat-Mangelsituation kann das Hirnödem verhindert werden.
Andere ödematöse Zustände, lokal oder generalisiert. Aufgrund des Absinkens der Nierenfunktion ab dem 25. bis 30. Lebensjahr um jeweils 10 % pro Dezennium kommt es häufig zu lokalen (Augenringe) oder generalisierten Flüssigkeits-Einlagerungen in den Körper , als erstes als Schwellung der abhängigen Partien, an den Knöcheln zu beobachten. Bandscheiben-Vorfälle, die in den Spinalkanal vordringen verursachen zudem lokale Entzündungen mit einem umgebenden sauren Milieu, was wiederum zur vermehrten Flüssigkeits-Einlagerung in das betroffene Gebiet führt. Durch ausreichende Einnahme von Natrium-Bikarbonat kann dagegen der Zustand der „Contraction-Alkalosis“ mit Minderung der Flüssigkeits-Einlagerung erzeugt werden, was zur Besserung der neurologischen Symptome wie Schmerzen und Lähmungserscheinungen durch die spinale Dekompression führt.
Relativ gut bekannt ist auch die bei Diabetes bei schlechter Einstellung der Diät oder bei Insulinmangel vorkommende, diabetische Azidose. Logischerweise sollte auch dort der herrschende Bikarbonat-Mangel behoben werden, was die diätetische oder die Einstellung mit Insulin ergänzen und erleichtern würde, was bisher aber von Diabetologen vernachlässigt wird. Noch weniger oder gar nicht bekannt ist, dass eine konsequente Kompensation des chronischen Bikarbonat-Defizits auch die gefürchteten Gefäßschäden bei Diabetikern, die zu Amputationen, Nierenversagen mit Dialysepflichtigkeit oder zur Erblindung führen, aufgrund der Durchblutungsverbesserung wenn nicht verhindern, so doch aber signifikant hinauszögern kann. Wenn schon nicht allein das katastrophale, persönliche Schicksal der Betroffenen Grund genug wäre, die flankierende Prophylaxe mithilfe der Zufuhr von wohlfeilen Bikarbonat-Präparaten durchzuführen, so wäre dies, sozioökonomisch gesehen, sicher auch billiger als eine chronische Dialysebehandlung, die pro Woche rund tausend Euro kostet.
Osteoporose
Ähnlich, aber pathophysiologisch noch weitgehend unbekannt und unverstanden sind die Verhältnisse bei der Prophylaxe der Alters-Osteoporose. Auch hier wird wieder die alles dominierende Rolle des Milieu interieur, à la Claude Bernard speziell des Säure-Basen-Gleichgewichts, deutlich. Persönliche klinische und wissenschaftliche Erfahrungen des Autors, weisen darauf hin, dass bei Azidose die Homöostase der Knochen-Kollagen-Matrix durch den Ausstrom der Mineralsalze aus dem Knochen in Richtung eines erhöhten Knochen-Abbaus verschoben wird (= Katabolie), während gut gefüllte Bikarbonat-Reserven den Knochenmineralsalzbestand durch den Einbau von Calcium-Salzen in die Knochengrundsubstanz begünstigen (=Anabolie) und daher eine Osteoporose verhindern können. Ebenfalls ein Grund mehr, die jährlichen Milliarden, die diese Volkskrankheit kostet, dadurch zu vermindern, dass Bikarbonat täglich, dauerhaft und ausreichend substituiert wird.
Malignom-Entstehung, Wachstum und Metastasierung. Prophylaxe und Behandlung, Unterstützung der Chemotherapie und Bestrahlung durch Ausgleich des BDS.
Gesichert ist, dass bei Malignomen das zelluläre Milieu deutlich sauer ist, d.h. die Malignom-Zelle proliferiert am besten in einer sauren Umgebung und weniger gut in einem basischen Milieu (Otto H. Warburg Hypothese). Daher ist denkbar, dass in einem chronisch sauren Milieu die sog. Carcinogenese, d.h. die Krebsentstehung begünstigt und in einem basischen Milieu gehemmt wird. Hierfür sprechen Untersuchungen an Vegetariern. Möglicher Grund hierfür ist, dass die sog. Immunsurveillance, (das ist der im Körper unentwegt für die Entfernung von entstehenden Krebszellen verantwortliche Abwehrmechanismus), bei Azidose nicht optimal arbeitet. Sicher ist, aufgrund entsprechender Erfahrungen des Autors, dass speziell bei Chemotherapie Malignompatienten sich in einer schweren Azidose befinden wie systematische Messungen ergeben haben. Dieses typische Bikarbonat-Defizit-Sydrom kann durch optimalen Säure-Basen-Ausgleich, d.h. durch reichliche Bikarbonat-Substitution bis zu dem empfohlenen Urin-pH behoben werden und die Nebenwirkungen von Chemotherapien und Bestrahlungen werden deutlich verringert und die typischerweise durch nephrotoxische Chemotherapeutika drohenden nephrotoxische Schäden bis hin zum Akuten Nierenversagen können vermieden werden.
Sport, Hochleistungssport, Muskel-Tätigkeit
Die Muskeln sind die Bewegungsorgane des menschlichen Körpers, wobei die quergestreifte Skelettmuskulatur das größte parenchymatöse Organ mit einem Anteil von 25 % bis 40 % des Körpergewichts darstellt. Die Muskeln der Extremitäten führen schnelle Bewegungen von großer Amplitude aus, die Rückenmuskulatur erfüllt vorwiegend Haltefunktionen. Der Stoffwechsel des ruhenden Muskels ist niedrig und wird fast vollständig durch den aeroben Abbau von Kohlehydraten gedeckt. Für Kontraktionen der Muskulatur wird (vereinfacht, zusammengefaßt) die Energie aus dem oxidativen Abbau von unveresterten Fettsäuren und Glukose sowie aus gespeichertem Glykogen gewonnen. Hierbei entstehen energiereiche Phosphatverbindungen, gleichzeitig reichert sich Milch-Säure im Mycoplasma der Muskelzelle an. Bei einem dort auf 6,4 abgesunkenen pH-Wert wird der Muskel-Stoffwechsel und damit die Leistung blockiert. Durch den Glykogen- und Glukose-Abbau zur Energiegewinnung entsteht letztendlich Kohlen-Säure (CO2), die ohne ausreichende Abatmung ebenfalls zur Übersäuerung des gesamten Körpers führt (respiratorische Azidose). Typischerweise führen sich Sportler, besonders bei gefragten Höchstleistungen hochkalorische und proteinreiche sog. „Energie-Drinks“ zu. Hierdurch wird die täglich anfallende Menge von 40 bis 80 mMol von sog. fixen sauren Stoffwechsel-Endprodukten noch deutlich gesteigert. Auch die junge, gesunde Niere kann nur einen maximal sauren Urin-pH von 4,5 produzieren. Was im Körper verbleibt, führt zur metabolischen Azidose mit einem entsprechendem Mangel an NaHCO3. Sportliche Höchstleistungen führen daher durch den erhöhten Anfall von CO2 und Milchsäure in der Muskulatur unweigerlich zu einer drastischen Übersäuerung (=Azidose). Diese kann nur durch entsprechende Zufuhr von NaHCO3 neutralisiert werden. Gleichzeitig wird aufgrund der oben geschilderten, verbesserten Nierenphysiologie die Ausscheidung der Stoffwechsel-Säuren im Urin optimiert. Ein Grund mehr für die durch positive praktische Erfahrungen gestützte Zufuhr von NaHCO3 beim Sport.
Nach diesen zahlreichen Verweisen auf wissenschaftliche Zusammenhänge, Erkenntnisse und Fakten, mag auch verständlich werden, dass die Erkenntnisse des Autors über den anzustrebenden Messwert des Säure-Basen-Haushalts, d.h. das anzustrebende pH-Optimum und die daraus resultierenden Schlussfolgerungen erst nach über 30-ig jähriger intensiver wissenschaftlicher und klinischer Beschäftigung mit diesem Thema gewonnen werden konnten.
Diskussion
Neben dem Bikarbonat-Mangel können noch andere Mangel-Syndrome bestehen z.B. Jod, Eisen oder Hormon-Mangel etc. die altersbedingt oder durch die heutigen Lebensumstände wie eingangs geschildert, bedingt sind.
Unser Organismus, der eines landlebenden Säugers, ist ein hoch komplexer Bioreaktor, in dem ungezählte organisch-chemische Prozesse gleichzeitig ablaufen. Hierfür ist aber die eingangs erwähnte Konstanz des „milieu interne“ (Claude Bernard) wie z.B die Körpertemperatur und das Säure-Basen-Gleichgewicht unabdingbar. Die bioreaktiven Prozesse werden durch hormonelle und neuronale Stimuli oder Bremsen gesteuert und von Katalysatoren beschleunigt. Vitamine, Enzyme, Spurenelemente, Puffersysteme, Sauerstoff und CO2 sowie die Konzentrationen der reagierenden Substrate und deren Metabolite und die Temperatur beeinflussen, je nach ihrer Konzentration, die Reaktionsabläufe. Entsteht irgendwo endogen oder exogen ein Defizit oder eine Mangelsituation verändern sich notgedrungen die Prozeßabläufe in der einen oder anderen Richtung.
In den seltensten Fällen kann daher eine Fehlreaktion, ein krankhafter Zustand, d.h. eine Krankheit nur auf einen einzigen Mangelzustand zurückgeführt werden. Hierdurch werden aber die verschiedensten Interpretationen und Lehrmeinungen von Krankheiten verständlich, die sich Betrachtern mit unterschiedlicher Wahrnehmung ihrer fachspezifischen Aspekte als einzige Ursache darstellen. Diese Vereinfachung ist aber aufgrund der oben geschilderten Komplexität und Vielfalt der Reaktionsabläufe im Organismus nicht zulässig, „terrible simplificateurs“. Leider beruhen hierauf sowohl einseitige bornierte sogar bösartige Prognosen als auch Wunderheilung verkündende Botschaften mit entsprechenden Wunderdrogen. Erstere besitzen keine fundierte Gültigkeit und die Drogen können in verschiedenen Situationen schädlich oder toxisch sein.
Im Falle des Bikarbonat-Mangels bzw. des Bicarbonate-Deficit-Syndroms, BDS ist das wichtigste Puffersystem des Organismus d.h. die biochemische Säure-Basen-Balance, also die Konzentration zwischen H+ und OH- Ionen betroffen. Wie die Körpertemperatur müssen diese Konzentrationen in engen Grenzen konstant bleiben, da sie eine wichtige Basis für die physiologischen Reaktionsabläufe bilden. Es ist daher sinnvoll einen Bikarbonat-Mangel immer auszugleichen, sobald er erkannt wird. Alters- oder Zivilisations- bedingt und krankheitsbegleitend ist der Bikarbonat-Mangel wesentlich häufiger als gemeinhin angenommen wird.
Zusammenfassung
Der praktische Nutzen einer optimalen Bikarbonat-Substitution ist immens, fast grenzenlos. Osteoporose, Gicht, Komplikationen in der Schwangerschaft (Eklampsie, EPH-Gestosen), durch schwere Verletzungen (= Polytrauma) z.B. die Schwellung des Gehirns bei Schädelhirn-Trauma, des Rückenmarks bei Wirbelsäulenversetzungen, Schweregrad und Folgeschäden von Diabetes, Bluthochdruck, Einsatz von Dialyse bei Akutem und Chronischem Nierenversagen, Unverträglichkeit und Folgen von Chemotherapie und vieles andere mehr sind in einem bisher ungeahnten Maße vermeidbar.
Spenderorgane bleiben über einen bisher nicht bekannten Zeitraum hinaus vital und sind daher in erhöhtem Maße verfügbar. (Siehe Artkel: ANV- Die Kopp’sche Lösung)
Wirkung und Nutzen der Nahrungsergänzung mit Natriumbikarbonat sind aufgrund alter, teils vergessener und neuerer, noch unbekannter oder unverstandener Erkenntnisse noch nicht voll ausgeschöpft. Die naturheilkundlichen und erfahrungsmedizinischen Empfehlungen zur „Verbesserung“ des Säure-Basen-Gleichgewichts zeigen, dass in der Menschheit ein Gespür dafür vorhanden ist, dass eine Mangelsituation (BDS) besteht, die nach Ausgleich verlangt.
Anhang
Für den eingangs erwähnten Natrium- Irrtum sind folgende Informationen erforderlich
Biochemie: Böses Natrium? - Gutes Natrium?
Es gibt streng genommen kein für sich allein vorkommendes Natrium-Ion oder Na+ in der Natur. Im Reagenzglas unter besonderen Aufbewahrungsbedingungen ja, da ist es ein weißglänzendes Metall, das allerdings in der Luft sofort verbrennen würde. Na+ ist normalerweise immer an irgendein negativ geladenes Kation z.B. Cl- oder HCO3- gebunden und heißt dann NaCl = Kochsalz oder NaHCO3 = Natriumhydrogencarbonat oder Natriumbikarbonat. Diese beiden Substanzen haben grundverschiedene Wirkungen, teilweise entgegengesetzte im Organismus. NaCl kann schädlich „böse“ sein. Natriumbikarbonat ist als physiologischer Puffer in der richtigen Konzentration immer GUT.
Kein Mensch kommt hoffentlich auf die Idee, hundert 1-Gramm Tabletten Natriumbikarbonat oder 100 Gramm NaHCO3 oder noch mehr als Pulver auf einmal zu schlucken, das geht nicht gut.
Natrium für sich allein ist also weder gut noch böse, sondern nur in der Bindung mit Chlorid oder Hydrogenkarbonat.
Irreführend ist, dass selbst in der wissenschaftlichen Medizin Natrium einfach gleich Kochsalz (= NaCl) gesetzt wird. Tatsächlich wird unentwegt selbst in hochkarätigen wissenschaftlichen Arbeiten mit anderer Thematik meist nur von Natrium gesprochen, wenn NaCl also Kochsalz gemeint ist. Dadurch ist die Verwechslung mit anderen Natrium-Salzen leider vor allem mit Natrium-Bikarbonat vorprogrammiert Da aber niemand zu viel Salz essen soll, schon gar nicht Herz-, Nieren- oder Hochdruck-Kranke, auch nicht Schwangere, d.h. gar niemand, - wird verzweifelt versucht, den gesamten Natrium-Gehalt von Mineralwässern oder verschiedenen Nahrungsmitteln oder Diätetika, so niedrig wie möglich zu halten und kostenaufwendig zu entfernen oder zu reduzieren, damit ja nur kein Schaden entsteht. Deshalb steht auf dem Mineralwasser- Etikett immer "Natrium-arm". Richtigerweise müsste es "Kochsalz-arm" heißen, nur leider ist auch das ebenfalls reduzierte Natrium-Bikarbonat von der "Natrium-Verarmung" mit betroffen.
Das ist in vielerlei Hinsicht ein sehr kostspieliger Fehler und Irrtum.
PS Vertraulich: Die in dem Artikel als neue Erkenntnisse des Autors gekennzeichnete Angaben sind markenzeichenrechtlich geschützt